Infertilité et Endometriose
Mis à jour le 30/04/2021
Dr Emmanuelle Mathieu d’Argent
Praticien Hospitalier, Responsable de l’Unité fonctionnelle d’AMP, Préservation de la fertilité et chirurgie de l’infertilité. Service de gynécologie Obstétrique et Médecine de la Reproduction, Hôpital Tenon, Assistance Publique- Hôpitaux de Paris. Université Pierre et Marie Curie Paris 6. GRC6-UPMC : Centre Expert en Endometriose (C3E), France.
Pour le Groupe de travail du réseau de soin Endométriose AP-HP IdF *
* Groupe de travail du réseau de soin Endométriose APHP IdF : N AFLAK, A AGMAN, J-M. ANTOINE, A ARFI, M BAZOT, S BENDIFALLAH, J-L BENIFLA, F BONNET, B BORGHESE, A-C BORDONNE, G CANLORBE, P CAPMAS, L CARBILLON, I CEDRIN- DURNERIN, N CHABBERT BUFFET, C DARAÏ , E DARAÏ, X DEFFIEUX, L DURANTEAU, S EPELBOIN , F EUSTACHE, M EVEN , A FAUCONNIER, A FAZEL , H FERNANDEZ, G GALULA, L GRIMALDI, M GRYNBERG, C HUCHON, C HASSEN-KHODJA, M KOSKAS, F LECURU, J-M LEVAILLANT, R LEVY, L MAITROT, E MATHIEU d’ARGENT, A-E MILLISCHER-BELLAICHE, M PEIGNE, G PLU-BUREAU, P SANTULLI, N SERMONDADE, J SROUSSI, N TARIGHT, I THOMASSIN-NAGGARA, A THOMIN, C TOUBOUL, P TOURAINE , C UZAN, E WAFO.
Introduction :
Maladie chronique, l’endométriose touche 6 à 10% des femmes en âge de procréer (1). Dans la population des femmes infertiles, la part de l’endométriose est difficile à évaluer et varie de 20 à 68 % selon les études (2). En cas d’endométriose avérée, les taux de fécondité par cycle sont abaissés et évalués à 2-10%, contre 25-30% au sein des couples fertiles, pour les 3 premiers cycles d’exposition (3).
La prise en charge de l’infertilité liée à la maladie endométriosique fait l’objet de multiples publications et de nombreuses controverses. En effet, de très nombreux facteurs interviennent dans le choix des propositions de traitement de l’infertilité : la sévérité de la maladie et les organes atteints, la symptomatologie douloureuse et l’efficacité du traitement médical, l’atteinte ovarienne (présence d’endométriomes, stigmates cliniques biologiques et échographiques d’altération de la réserve ovarienne) ou utérine (adénomyose) et les facteurs associés (tubaires, masculins..). La prise en charge de l’infertilité dans ce contexte de maladie endométriosique fait appel essentiellement à l’AMP et/ou à la chirurgie, de manière indépendante ou combinée, en association à des traitements antalgiques et hormonaux. La décision doit être, autant que possible, prise au sein de centres pluridisciplinaires, associant radiologues, chirurgiens gynécologues, spécialistes de l’AMP, et doit associer les couples, dans le cadre d’une décision médicale partagée, en Réunion de Concertation Pluridisciplinaire (RCP).
L’infertilité liée à l’endometriose :
Mécanismes
Les mécanismes de l’infertilité dans l’endométriose sont débattus, nombreux et très souvent intriqués. Ils peuvent être mécaniques (tubaires, par le biais d’adhérences, de rétractions fibreuses ou d’hématosalpinx), utérins (par altération de la réceptivité endométriale avec résistance à la progestérone, ou peut-être par le biais de l’adénomyose (5), liés à l’altération du capital ovocytaire ou à l’inflammation intra péritonéale et sa toxicité sur les gamètes. Enfin, les dyspareunies liées à l’endométriose peuvent expliquer également l’infertilité de fait de la raréfaction ou de l’absence de rapports sexuels.
Sur le plan clinique, l’association infertilité-endométriose est établie, avec des chances de conception naturelle faibles, en particulier dans les formes sévères de la maladie : le taux de grossesse spontanée en cas d’infertilité liée à une endometriose est de 36 % à 3 ans, versus 55% dans les infertilités inexpliquées (6). L’étude de Prescott (7) a montré un risque relatif ajusté d’infertilité de 1,78 en cas d’endometriose. Enfin une étude transversale en ligne menée au Canada entre 2018 et 2019 retrouvait 7% d’endometriose dans la population interrogée. Chez ces patientes, le taux d’infertilité était de 22% contre 6.3% dans le reste de la cohorte (8). Il est donc justifié de proposer une prise en charge à ces couples.
Facteurs associés
Avant toute prise en charge d’une infertilité en contexte d’endométriose, il est indispensable de proposer un bilan complet de l’infertilité comprenant en particuliers un bilan de réserve ovarienne et un spermogramme, ainsi qu’une cartographie complète des lésions d’endometriose. La demande spécifique du couple ainsi que le retentissement sur la qualité de vie de la patiente et l’efficacité des traitements hormonaux et antalgiques proposés rentrent en compte dans le choix thérapeutique. Cette décision peut être prise en Réunion de Concertation Pluridisciplinaire spécialisée.
Les traitements possibles
La prise en charge de l’infertilité n’est jamais univoque et combine les traitements médicaux et les prises en charges associées éventuelles, les techniques d’AMP et la chirurgie des lésions d’endométriose. Ces décisions doivent être réfléchies dans le temps, en intégrant dans la prise en charge sur le long terme les propositions éventuelles de préservation de fertilité, de traitement médical ou chirurgical, et d’AMP intraconjugale voir de don d’ovocytes si besoin.
Chirurgie
Les recommandations internationales ne sont pas homogènes : La société européenne pour la reproduction humaine et l’embryologie- ESHRE (9), laWorld Endometriosis Society et le National Institute for Health and Care Excellence- NICE (10) anglais estiment que la chirurgie améliore la fertilité spontanée dans les cas d’endometriose minime à modérée. Les recommandations italiennes- ETIC (11) préconisent quant à elles de ne pas réaliser de chirurgie chez ces mêmes patientes si le seul but en est l’amélioration de la fertilité. Les recommandations canadiennes proposent un traitement laparoscopique pour améliorer la fertilité spontanée dans les formes minimes ou légères, mais le discutent dans les formes profondes. Les recommandations françaises-CNGOF/HAS (12) ne proposent pas de traitement chirurgical dans le seul but d’améliorer la fertilité dans les formes sévères mais le discutent en cas d’échec d’AMP.
Si une décision chirurgicale est prise:
- Une chirurgie complète des lésions d’endométriose en première ligne peut être envisagée, dans le but de restaurer la fertilité spontanée et d’améliorer les chances de naissances vivantes, spontanément et après AMP. Ceci est discuté et une étude prospective multicentrique randomisée française est en cours (ENDOFERT) pour évaluer l’intérêt en première intention de la chirurgie ou de la FIV en cas d’endométriose profonde avec atteinte colorectale (Pr Collinet, CHRU de Lille).
La chirurgie a également été proposée pour améliorer les chances de grossesse en FIV après plusieurs échecs en AMP (13).
- On peut également discuter une chirurgie des seules lésions dont la présence pourrait compliquer la prise en charge en AMP, dans le but d’améliorer sa faisabilité, son efficacité (en particuliers en cas de lésions tubaires), sa tolérance (en diminuant les douleurs pelviennes en cas d’endométriomes ovariens volumineux par exemple) et/ou de diminuer les risques de complications de la FIV.
En revanche, il est maintenant admis que la chirurgie par kystectomie des endométriomes est délétère pour la fertilité en altérant la réserve ovarienne (14-15) et que la pratique de kystectomies pour endométriomes n’améliore pas les taux de naissance en FIV (Meta-Analyse de Hamdan, 16).
Cependant, le traitement chirurgical des endométriomes peut se discuter en cas de dysménorrhée sévère, de suspicion de lésion maligne, ou d’endométriomes très volumineux, pour améliorer l’accès aux follicules (17). Cette prise en charge permettrait également de d(18). On choisira dans ces cas les techniques les moins délétères (19destruction de la « paroi » interne du kystepar coagulation bipolaire, destruction par laser ou vaporisation par Plasmajet©.
En cas d’endométriome isolé (ce qui est peu fréquent) ou très prédominant dans la symptomatologie, les nouvelles thérapeutiques médicales doivent être envisagées, en particulier le recours au Dienogest (20). Ce traitement pourrait également limiter le risque de récidive après traitement chirurgical (21) et pourrait donc être utilisé à la fois comme traitement post opératoire et pré traitement à la FIV.
En cas d’hydro ou hématosalpinx, on pourra discuter la salpingectomie, en 1ere ou 2eme intention pour améliorer les chances de grossesse (22).
Les complications de la chirurgie doivent être également prises en compte dans la décision.
La chirurgie pour endométriose profonde avec atteinte colorectale expose les patientes à des risques de complications post opératoires : fistule anastomotique, vaginale, occlusion intestinale, hémorragie digestive, fistule urinaire, abcès pelvien ou dysurie postopératoire. Ce taux de complication est de 0 à 43% dans la méta-analyse de Meuleman (23).
Les stimulations simples de l’ovulation et les Inséminations Intra Utérines (IIU)
Il existe assez peu de publications concernant la pratique des IIU en contexte d’endométriose. Les points essentiels qui se dégagent de la littérature sont :
- La présence d’endométriose est un facteur de risque d’échec en IIU et les taux de succès sont faibles: 5,5% dans l’étude de Sicchieri (24).
- Les taux de succès des IIU sont identiques à ceux des infertilités inexpliquées uniquement en cas d’endométrioses légères à modérées (25).
- Les taux de succès sont identiques en protocole stimulé (avec ou sans blocage préalable) ou en cycle naturel, chez des patientes présentant une endométriose modérée (avec des taux cumulés de naissance de 18,5% après 3 cycles) (26).
Dans ce contexte, l’ASRM en 2012, l’ESHRE en 2014 et le CNGOF en 2017, recommandent la pratique de stimulations ovariennes avec ou sans IIU uniquement dans les formes légères ou modérées d’endométriose et dans un délai de 6 mois post chirurgie pour l’ESHRE (après validation du stade de la maladie et de la perméabilité d’au moins une trompe).
Le CNGOF ajoute que « les données de la littérature sont insuffisantes pour conclure sur la place des traitements d’AMP hors FIV dans les cas d’endométriose pelvienne profonde ou d’endométriomes ».
La Fécondation In Vitro (FIV)
Si les premières publications concernant les résultats de la FIV en cas d’endométriose relevaient des taux de succès inférieurs à ceux des autres indications, de nombreuses publications retrouvent globalement des taux de grossesse par cycle équivalents, toutes formes d’endometriose confondues (27). Cependant, plusieurs études très récentes montrent que l’endométriose est associée à des nombres d’ovocytes utiles recueillis à la ponction plus faibles que dans les autres indications (surtout en cas d’antécédent de chirurgie ovarienne), et donc à des taux cumulatifs de grossesse plus faibles que chez les témoins, essentiellement du fait d’un nombre plus faible d’embryons obtenus, sans altération de leur qualité (28).
En ce qui concerne la qualité embryonnaire, les études récentes ne montrent en effet pas d’altération en cas d’endométriose : les pourcentages d’embryons clivés et de blastocystes de bonne qualité sont identiques à ceux des groupes contrôles (29). De plus, l’étude des taux d’aneuploïdie ne retrouve pas de différence significative en cas d’endométriose, en comparaison avec les taux des contrôles (30-31).
En ce qui concerne le choix du protocole de stimulation ovarienne, il existe un certain consensus sur l’intérêt d’un pré traitement de blocage ovarien, par agonistes de la GnRH, traitement œstro-progestatifs ou certains progestatifs comme le dienogest (32-34).On pourra utiliser des protocoles agonistes ou antagonistes, un score de propension ayant montré des résultats similaires (35).
Certaines équipes proposent, en cas d’endometriose, le recours à des stimulations ovariennes avec blocage du pic de LH par progestatifs et transfert différé, avec des résultats en terme de naissance par transfert comparables (36) à ceux obtenus avec les protocoles de référence. Pour la FIV en contexte d’endometriose, les données sont encore récentes et méritent d’être confirmées.
Enfin, il n’existe actuellement aucune étude de bon niveau de preuve permettant de proposer des compléments nutritionnels ou le recours à une médecine « alternative » dans l’infertilité associée à l’endométriose, quel que soit son stade.
En ce qui concerne la stratégie de transfert, de nombreuses études ont maintenant montré que le transfert différé des embryons, privilégiant le transfert après vitrification par rapport au transfert d’embryons frais n’apportait pas d’amélioration des taux de grossesse cumulés, en population générale (37). Deux études récentes (38-39) montrent, sur de faibles effectifs, de meilleurs taux de naissances vivantes en cas de transfert d’embryons congelés chez des patientes atteintes d’endométriose. Ces résultats demandent à être confirmés par des études plus larges.
Les facteurs pronostics de la FIV en cas d’endométriose
En ce qui concerne le stade de l’endométriose, les études se contredisent. Dans une étude rétrospective récente (40) le phénotype endométriosique (endométriose superficielle, endométriomes, ou endométriose profonde) n’a pas d’impact sur les résultats en FIV. En revanche, l’altération de la réserve ovarienne ou les antécédents de chirurgie de l’endométriose, en particuliers ovarienne, sont associés à des taux plus faibles de grossesse.
Le rôle péjoratif de l’adénomyose reste très débattu. Cependant, la majorité des études montrent le rôle péjoratif de l’adénomyose sur les résultats en FIV, et la méta analyse de Vercillini en 2014 (41) retrouvait une baisse de 28% des taux de grossesse en cas d’adénomyose.
L’impact de la présence d’endométriomes en cours de stimulation pour FIV ne semble pas être un facteur péjoratif (16), y compris pour des tailles importantes : la présence d’endométriomes de moins de 6 cm laissés en place pendant la FIV n’aurait aucun impact ni sur la qualité embryonnaire, ni sur les taux de grossesse et de naissance.
Risques et complications
La pratique de la FIV dans l’indication « endométriose » est caractérisée par une bonne tolérance et des taux faibles de complications et effets secondaires. Ainsi, les stimulations ovariennes en vue de FIV ne semblent pas accélérer l’évolution de l’endométriose (42) ni augmenter les taux de récidive après chirurgie (43).
L‘étude de Benaglia en 2008 (43) montrait le caractère exceptionnel des abcès post ponction en contexte endométriosique (< 1,7%). Plusieurs études du même auteur ne rapportaient ni aggravation de la maladie endométriosique post FIV (RR d’aggravationOR= 0,92 (95% IC:0,77-1,10) (44), ni augmentation de la taille des endométriomes, ni difficultés particulières à la ponction en cas d’endométriomes en place (45) : à noter plus fréquemment une aspiration incomplète des follicules et donc un nombre d’ovocytes moindre que chez les témoins, mais pas de différence en terme de douleurs et d’aspiration post ponction d’ovocytes, quelle que soit la taille des endométriomes (supérieurs ou inferieurs à 27mm de diamètre). Enfin, l’évaluation de l’intensité des douleurs, et de la qualité de vie avant et après stimulation ovarienne pour FIV ne montrait pas d’exacerbation des symptômes, y compris chez des patientes présentant des lésions profondes (46). Cependant, des cas cliniques rapportent des complications post FIV, avec des perforations intestinales, des hémopéritoines, des abcès pelviens plus fréquents. Dans ce contexte, la Société Française d’Anesthésie Réanimation propose une antibioprophylaxie systématique lors de la ponction d’ovocytes en cas d’endométriose.
Obstétrique et Endometriose
Dans une très large revue de la littérature publiée par Leone Roberti Maggiore en 2016 (47), une association apparait comme vraisemblable entre endométriose et avortements spontanés, accouchements prématurés et retards de croissance intra-utérins. L’incidence des césariennes est plus élevée en cas d’endométriose.
La cohorte danoise publiée en 2017 par Glavind (48), comme la méta analyse de Lalani (49) confirmaient une augmentation du risque de prématurité, de prééclampsie et de césarienne en cas d’endometriose mais ces risques n’étaient pas modifiés en cas d’obtention de la grossesse par AMP. Sans les alarmer, il convient de prévenir les couples de l’importance d’un suivi obstétrical adapté.
Don d’ovocytes et endométriose
En cas d’échecs de FIV ou de réserve ovarienne très faible, le recours au don d’ovocytes est possible en contexte d’endométriose. Le pronostic en est cependant moins bon que chez les receveuses non atteintes, surtout en cas d’adénomyose associée : Martinez-Conejero (50) en 2011 ne retrouvait pas de différence significative entre les 3 groupes (témoins, receveuses atteintes d’endometriose sans adénomyose, receveuses atteintes d’endometriose avec adénomyose) pour les taux d’implantation et les taux de grossesse clinique entre les 3 groupes, mais une augmentation significative des taux de fausse couche et une diminution des grossesses à terme dans le groupe « adénomyose ».
Les stratégies de prise en charge
La prise en charge de ces patientes présentant une endométriose et une infertilité n’est pas univoque, elle doit être réfléchie et élaborée dans le temps, avec la patiente ou le couple, et combiner à la fois la prise en charge des symptômes, de la qualité de vie, et de la fertilité, en articulant la chirurgie, l’AMP (intra conjugale ou par don d’ovocytes), le recours à un traitement médical, et éventuellement à une préservation de fertilité.
Pour aider à la décision, un score de prédiction de grossesse spontanée post chirurgie a été établi par Adamson en 2010 (score Endometriosis Fertility Index) (51). Boujenah (52) a montré en 2017 que l’utilisation de ce score lors d’une coelioscopie diagnostique permettait d’adapter la stratégie thérapeutique et de proposer d’emblée des prises en charges en FIV en cas de score défavorables. En cas de scores favorables, les taux de grossesse rapportés, pour des grossesses spontanées et /ou par stimulation ovarienne hors FIV, étaient de 87,7% à 3 ans.
Sur le plan médico économique, Ferrier (53) a proposé une évaluation des différentes stratégies induites par l’utilisation du score EFI pour l’obtention d’une grossesse après coelioscopie pour endométriose. L’auteur concluait à l’intérêt médico économique majeur de cette stratégie de chirurgie première avec classification EFI pour déterminer les stratégies d’expectative ou de FIV les plus efficientes.
En considérant les performances des différentes stratégies, les risques et complications inhérents à la chirurgie et la Fécondation in Vitro, les données de la littérature ici exposées et les recommandations françaises de 2017, les stratégies suivantes peuvent être proposées :
Chez des femmes jeunes, en cas d’endométriose superficielle ou modérée, avec perméabilité tubaire conservée, en l’absence de facteurs masculins défavorables ou de réserve ovarienne altérée, 2 à 3 cycles de stimulation ovarienne par gonadotrophines peuvent être proposés, éventuellement associés à des inséminations intra-utérines. En dehors de ces situations, ou en cas d’échec, le recours à la FIV ou à la chirurgie des lésions d’endométriose (en épargnant au maximum la réserve ovarienne), doivent être envisagés. Les arbres décisionnels (figures 1 et 2) présentés ici ont été proposés par notre groupe de travail de l’APHP en 2019.
CONCLUSION :
Multidisciplinaire par essence, la prise en charge de l’infertilité présente ou future des patientes présentant une endométriose est un défi d’aujourd’hui, du fait de la prévalence accrue de l’endométriose, et de son impact majeur sur la fertilité des patientes atteintes. L’Aide Médicale à la Procréation a une place importante dans le traitement des patientes infertiles atteintes, essentiellement par le biais des techniques de Fécondation In Vitro, en association ou non avec la chirurgie pelvienne. En cas d’endometriose, la FIV offre a priori des taux de grossesse globalement équivalents à ceux qui sont obtenus dans les autres indications, quel que soit le stade de l’endométriose, malgré une altération fréquente de la réserve ovarienne liée à la maladie elle-même et à l’impact des chirurgies ovariennes. Si l’endometriose est responsable d’une diminution du nombre d’ovocytes recueillis après stimulation pour FIV, les études récentes montrent que la qualité embryonnaire n’est pas altérée, avec des taux de naissance par transfert et des taux d’aneuploïdie comparables à ceux des contrôles. Les études récentes concernant les risques de complications de l’AMP ou d’aggravation de la maladie sont rassurantes. Les modalités pratiques de la stimulation ovarienne (protocole agoniste ou antagoniste, prétraitement) et du transfert (frais ou différé) restent débattues, avec probablement un intérêt majeur à la mise en place d’un prétraitement. En cas d’insuffisance ovarienne avérée, et/ou d’échecs de FIV, le recours au don d’ovocytes peut être proposé. Enfin, depuis la loi de bioéthique 2011et l’autorisation de recourir à la préservation de fertilité « (lorsque) la fertilité risque d’être prématurément altérée », le recours à ces techniques peut être proposé en cas d’endométriose.
Figure 1 :
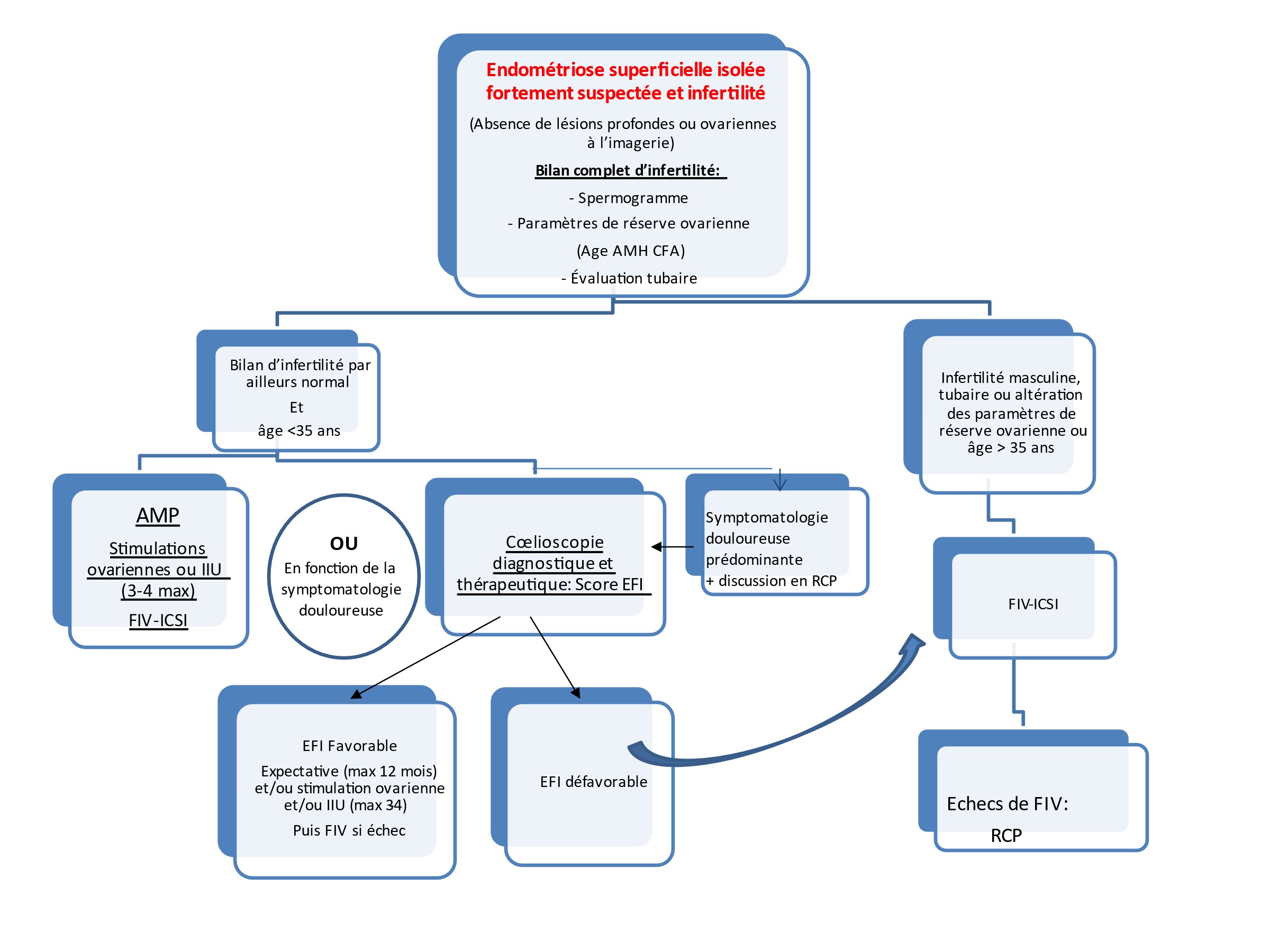
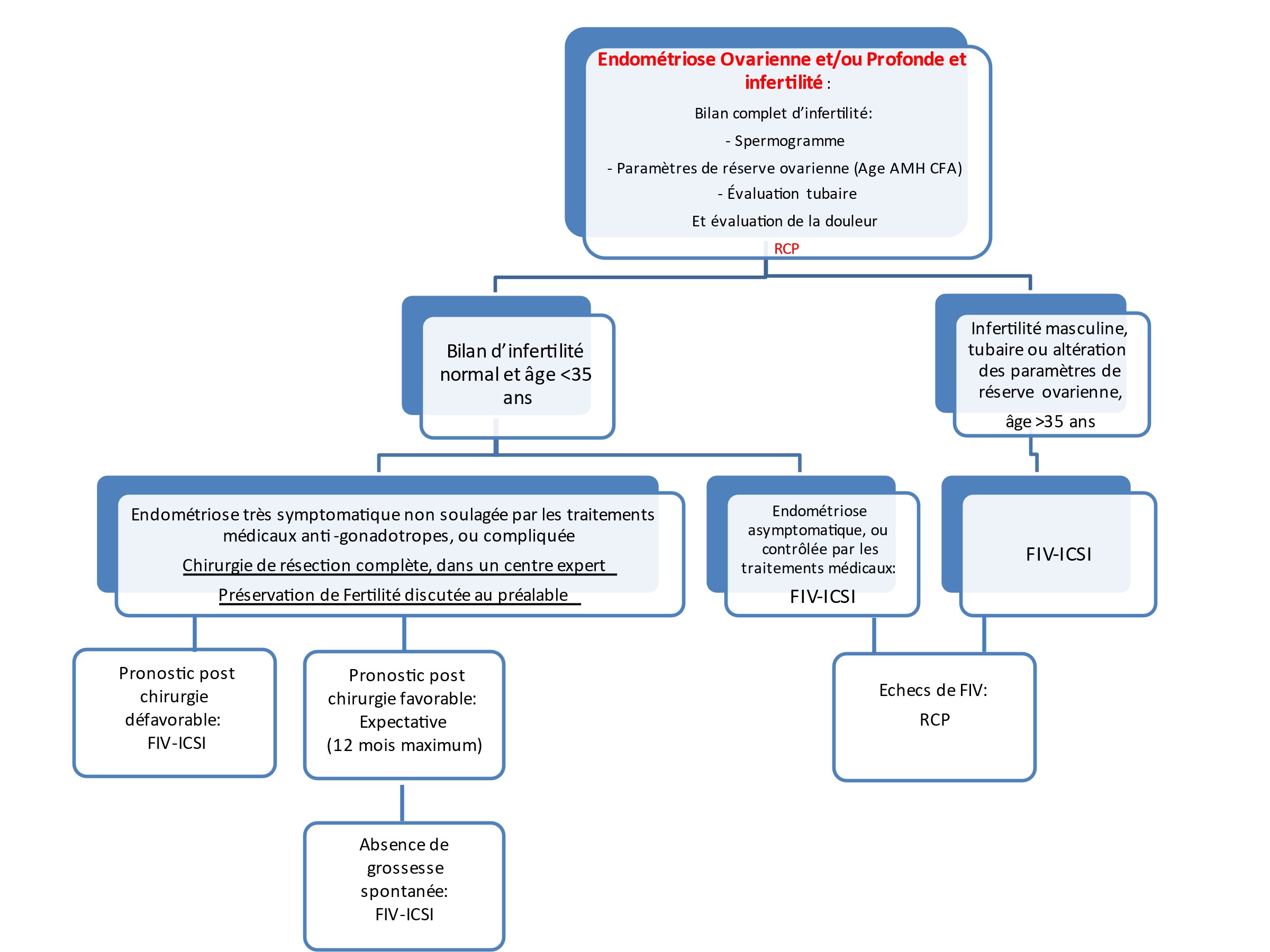
Figure 2 :
Références :
- Eskenazi B, Warner ML. Epidemiology of endometriosis.Obstet Gynecol Clin North Am : 1997 Jun;24(2):235-58.
- Mahmood TA, Templeton A. Prevalence and genesis of endometriosis. Hum Reprod. 1991 Apr;6(4):544-9.
- Gupta S, Goldberg JM, Aziz N, Goldberg E, Krajcir N, Agarwal A. Pathogenic mechanisms in endometriosis-associated infertility. Fertil Steril. 2008 Aug;90(2):247-57.
- Borghese B, Santulli P, Marcellin L, Chapron C.Borghese B, et al. Definition, description, clinicopathological features, pathogenesis and natural history of endometriosis: CNGOF-HAS Endometriosis Guidelines. Gynecol Obstet Fertil Senol. 2018 Mar;46(3):156-167.
- M, Marie-Madeleine Dolmans , Olivier Donnez , Hideaki Masuzaki , Michelle Soares , Jacques Donnez Enhanced follicular recruitment and atresia in cortex derived from ovaries with endometriomas Fertil Steril . 2014 Apr;101(4):1031-7.
- VA, Linda P Hunt, David J Cahill, Julian M Jenkins Differences in time to natural conception between women with unexplained infertility and infertile women with minor endometriosis Hum Reprod . 2004 Jan;19(1):96-103.
- Prescott J, Farland LV, Tobias DK, Gaskins AJ, Spiegelman D, Chavarro JE, Rich-Edwards JW, Barbieri RL, Missmer SA.Prescott J, et al. A prospective cohort study of endometriosis and subsequent risk of infertility. Hum Reprod. 2016 Jul;31(7):1475-82
- Singh S, Soliman AM, Rahal Y, et al. Prevalence, symptomatic Burden, and diagnosis of endometriosis in Canada: cross-sectional survey of 30 000 women/ Obstet Gynaecol Can 2020; S1701216319309806.
- GA, Vermeulen N, Becker C, Calhaz-Jorge C, D'Hooghe T, De Bie B, Heikinheimo O, Horne AW, Kiesel L, Nap A, Prentice A, Saridogan E, Soriano D, Nelen W; European Society of Human Reproduction and Embryology. Hum Reprod. 2014 Mar;29(3):400-12.
- Overview endometriosis: diagnosis and management Guidance NICE Internet, Cité 3 septembre 2019, https//www.nice.org.uk/guidance/ng73.
- ETIC. Endometriosis treatment Italian Club. When more is not better: 10”don’t’s”in endometriosis management. An ETIC position statement. Hum Reprod Open. 2019;2019(3): ho z009.
- Collinet P, Fritel X, Revel-delhomC et al. Management of endometriosis : CNGOF/HAS clinical practice guidelines –Short version. J Gynecol Obstet,Hum Reprod 2018.
- Soriano D, Adler I, Bouaziz J, Zolti M, Eisenberg VH, Goldenberg M, Seidman DS, Elizur SE.Soriano D, et al. Fertility outcome of laparoscopic treatment in patients with severe endometriosis and repeated in vitro fertilization failures.Fertil Steril. 2016. oct;106(5):1264-1269
- F, Metwally M, Amer S. The impact of excision of ovarian endometrioma on ovarian reserve: a systematic review and meta-analysis J Clin Endocrinol Metab 2012 Sep;97(9):3146-54.
- Hong SB, Lee NR, Kim SK, Kim H, Jee BC, Suh CS, Kim SH, Choi YM.Hong SB, et al. In vitro fertilization outcomes in women with surgery induced diminished ovarian reserve after endometrioma operation: Comparison with diminished ovarian reserve without ovarian surgery. . Obstet Gynecol Sci. 2017 Jan;60(1):63-68.
- Hamdan M, Dunselman G, Li TC, Cheong Y. The impact of endometrioma on IVF/ICSI outcomes: a systematic review and meta-analysis. Hum Reprod Update. déc 2015;21(6):809‑25.
- Park HJ, Kim H, Lee GH, Yoon TK, Lee WS.Park HJ, et al. Could surgical management improve the IVF outcomes in infertile women with endometrioma?: a review. Obstet Gynecol Sci. 2019 Jan;62(1):1-10.
- L, Somigliana E, Iemmello R, Colpi E, Nicolosi AE, Ragni G. Endometrioma and oocyte retrieval-induced pelvic abscess: a clinical concern or an exceptional complication? Fertil Steril. 2008 May;89(5):1263-6.
- N, H Roman, G Mage, M Canis Surgery for the management of ovarian endometriomas: from the physiopathology to the pre-, peri- and postoperative treatment. Gynecol Obstet Fertil Actions. 2011 Dec;39(12):709-21
- Angioni S, Pontis A, Malune ME, Cela V, Luisi S, Litta P, Vignali M, Nappi L.. Is dienogest the best medical treatment for ovarian endometriomas? Results of a multicentric case control study. Gynecol Endocrinol. 2020 Jan;36(1):84-86.
- Zakhari A, Edwards D, Ryu M, Matelski JJ, Bougie O, Murji A. Dienogest and the Risk of Endometriosis Recurrence Following Surgery: A Systematic Review and Meta-analysis. J Minim Invasive Gynecol. 2020 Nov-Dec;27(7):1503-1510.
- Dechaud H.. Hydrosalpinx and ART: hydrosalpinges suitable for salpingectomy before IVF. Hum Reprod. 2000 Dec;15(12):2464-5.
- Meuleman C, Tomassetti C, D'Hoore A, Van Cleynenbreugel B, Penninckx F, Vergote I, D'Hooghe T Surgical treatment of deeply infiltrating endometriosis with colorectal involvement. . Hum Reprod Update. 2011 May-Jun;17(3):311-26.
- F, Bomfim Silva A, et al Prognostic factors in intrauterine insemination cycles. JBRA Assist Reprod . 2018 Mar 1;22(1):2-7.
- E, Carl Spiessens, Christel Meuleman, Thomas D'Hooghe No difference in cycle pregnancy rate and in cumulative live-birth rate between women with surgically treated minimal to mild endometriosis and women with unexplained infertility after controlled ovarian hyperstimulation and intrauterine insemination. Fertil Steril . 2006 Sep;86(3):566-71.
- van der Houwen LE, Schreurs AM, Schats R, Heymans MW, Lambalk CB, Hompes PG, Mijatovic V Efficacy and safety of intrauterine insemination in patients with moderate-to-severe endometriosis. Reprod Biomed Online. 2014 May;28(5):590-8.
- Mathieu d’Argent E, Coutant C, Ballester M, et al. Results of first in vitro fertilization cycle in women with colorectal endometriosis compared with those with tubal or male factor infertility. Fertil Steril 2010; 94:2441–3.
- Boucret L, Bouet PE, Riou J, Legendre G, Delbos L, Hachem HE, Descamps P, Reynier P, May-Panloup P.Boucret L, et al. Endometriosis Lowers the Cumulative Live Birth Rates in IVF by Decreasing the Number of Embryos but Not Their Quality. J Clin Med. 2020 Aug 1;9(8):2478.
- Sanchez AM, Pagliardini L, Cermisoni GC et al Does endometriosis influence the embryo quality and/or development ?Insights from a large retrospective matched cohort study. Diagnostics (Basel)2020 ; 10(2).
- Juneau C, Kraus E, Werner M, Franasiak J, Morin S, Patounakis G, Molinaro T, de Ziegler D, Scott RT Patients with endometriosis have aneuploidy rates equivalent to their age-matched peers in the in vitro fertilization population. Fertil Steril. 2017 Aug;108(2):284-288.
- Vaiarelli A, Venturella R, Cimadomo D, Conforti A, Pedri S, Bitonti G, Iussig B, Gentile C, Alviggi E, Santopaolo S, Zullo F, Rienzi L, Ubaldi FM Endometriosis shows no impact on the euploid blastocyst rate per cohort of inseminated metaphase-II oocytes: A case-control study. Eur J Obstet Gynecol Reprod Biol. 2021 Jan;256:205-210.
- Muller V, Kogan I, Yarmolinskaya M, Niauri D, Gzgzyan A, Aylamazyan E.Muller V, et al. Dienogest treatment after ovarian endometrioma removal in infertile women prior to IVF. Gynecol Endocrinol. 2017;33(sup1):18-21.
- Barra F, Laganà AS, Scala C, Garzon S, Ghezzi F, Ferrero S.Pretreatment with dienogest in women with endometriosis undergoing IVF after a previous failed cycle. Reprod Biomed Online. 2020 Nov;41(5):859-868
- Tamura H, Yoshida H, Kikuchi H, Josaki M, Mihara Y, Shirafuta Y, Shinagawa M, Tamura I, Taketani T, Takasaki A, Sugino N.The clinical outcome of Dienogest treatment followed by in vitro fertilization and embryo transfer in infertile women with endometriosis. J Ovarian Res. 2019 Dec 12;12(1):123.
- Rodriguez-Purata J, Coroleu B, Tur R, Carrasco B, Rodriguez I, Barri PN. Endometriosis and IVF: are agonists really better? Analysis of 1180 cycles with the propensity score matching. Gynecol Endocrinol Off J Int Soc Gynecol Endocrinol. sept 2013;29(9):859‑62.
- Guo H, Li J, Shen X, Cong Y et al. Efficacy of different progestins in women with advanced endometriosis undergoing controlled ovarian hyperstimulation for in vitri fertilization6 A single Centir Non inferiority Randomized Controlled Trial. Frontiers of Endocrinology March 2020(11) 1-10.
- Roque M, Haahr T, Geber S, Esteves SC, Humaidan P Fresh versus elective frozen embryo transfer in IVF/ICSI cycles: a systematic review and meta-analysis of reproductive outcomes. Hum Reprod Update. 2019 Jan 1;25(1):2-14.
- Bourdon M, Santulli P, Maignien C, Gayet V, Pocate-Cheriet K, Marcellin L, Chapron C The deferred embryo transfer strategy improves cumulative pregnancy rates in endometriosis-related infertility: A retrospective matched cohort study. PLoS One. 2018 Apr 9;13(4):e0194800.
- Wu J, Yang X, Huang J, Kuang Y, Wang Y.Fertility and Neonatal Outcomes of Freeze-All vs. Fresh Embryo Transfer in Women With Advanced Endometriosis. Front Endocrinol (Lausanne). 2019 Nov 8;10:770
- Maignien C1, Santulli P2, Gayet V1, Lafay-Pillet MC1, Korb D1, Bourdon M1, Marcellin L3, de Ziegler D1, Chapron C3. Prognostic factors for assisted reproductive technology in women with endometriosis-related infertility. Am J Obstet Gynecol. 2017 Mar;216(3):280.
- Vercellini P, Consonni D, Dridi D, Bracco B, Frattaruolo MP, Somigliana E. Uterine adenomyosis and in vitro fertilization outcome: a systematic review and meta-analysisHuma Reprod 2014, 29(5),964-977.
- Surrey ES. Endometriosis-Related Infertility: The Role of the Assisted Reproductive Technologies. Biomed Res Int. 2015;2015:482959.
- L, Somigliana E, Iemmello R, Colpi E, Nicolosi AE, Ragni G. Endometrioma and oocyte retrieval-induced pelvic abscess: a clinical concern or an exceptional complication? Fertil Steril. 2008 May;89(5):1263-6.
- L, Edgardo Somigliana, Paolo Vercellini, Francesca Benedetti, Roberta Iemmello, Valentina Vighi, Giulia Santi, Guido Ragni The impact of IVF procedures on endometriosis recurrence.Eur J Obstet Gynecol Reprod Biol 2010 Jan;148(1):49-52.
- Laura Benaglia 1 , Andrea Busnelli 2 , Rossella Biancardi 2 , Walter Vegetti 3 , Marco Reschini 3 , Paolo Vercellini 2 , Edgardo Somigliana 2 Oocyte retrieval difficulties in women with ovarian endometriomas Reprod Biomed Online . 2018 Jul;37(1):77-84.
- Santulli P, Bourdon M, Presse M, Gayet V, Marcellin L, Prunet C, de Ziegler D, Chapron C. Endometriosis-related infertility: assisted reproductive technology has no adverse impact on pain or quality-of-life scores. Fertil Steril. 2016 Apr;105(4):978-987.
- Leone Roberti Maggiore U, Ferrero S, Mangili G, Bergamini A, Inversetti A, Giorgione V, Viganò P, Candiani M. A systematic review on endometriosis during pregnancy: diagnosis, misdiagnosis, complications and outcomes. Hum Reprod Update. 2016 Jan-Feb;22(1):70-103.
- Maria Tølbøll Glavind 1 , Axel Forman 2 , Linn Håkonsen Arendt 3 , Karsten Nielsen 4 , Tine Brink Henriksen 5 Endometriosis and pregnancy complications: a Danish cohort study.Fertil Steril 2017 Jan;107(1):160-166.
- S Lalani, A J Choudhry , B Firth , V Bacal , Mark Walker , S W Wen , S Singh , A Amath , M Hodge , I Chen. Endometriosis and adverse maternal, fetal and neonatal outcomes, a systematic review and meta-analysis Hum Reprod. 2018 Oct 1;33(10):1854-1865.
- Martínez-Conejero JA, Morgan M, Montesinos M, Fortuño S, Meseguer M, Simón C, Horcajadas JA, Pellicer A Adenomyosis does not affect implantation, but is associated with miscarriage in patients undergoing oocyte donation. Fertil Steril. 2011 Oct;96(4):943-50.
- Adamson GD, Pasta DJ.Endometriosis fertility index: the new, validated endometriosis staging system. Fertil Steril. 2010 Oct;94(5):1609-15.
- Boujenah, J., Cedrin-Durnerin, I., Herbemont, C., Sifer, C., Poncelet, C. Non-ART pregnancy predictive factors in infertile patients with peritoneal superficial endometriosis. EJOGBR, March 2017 10.1016/j.ejogrb.2017.03.008
- Ferrier C, Boujenah J, Poncelet C, Chabbert-Buffet N, Mathieu D'Argent E, Carbillon L, Grynberg M, Darai E, Bendifallah S Use of the EFI score in endometriosis-associated infertility: A cost-effectiveness study. Eur J Obstet Gynecol Reprod Biol. 2020 Oct;253:296-303.

