Le bon développement du cerveau repose fortement sur un processus appelé la N-glycosylation, qui désigne l’ajout de sucres sur les protéines de l’organisme. Une altération de ce processus provoque un groupe très hétérogène de troubles métaboliques héréditaires, les troubles congénitaux de la glycosylation (CDG). Alors que toutes les cellules du corps sont concernées, les patients présentent dans la majorité des cas une atteinte essentiellement neurologique.
L’équipe des Dr Vincent Cantagrel et Laurence Colleaux, co-directeurs du laboratoire de « Génétique des troubles du neurodéveloppement » à l’Institut Imagine à l’hôpital Necker Enfants-malades AP-HP, a découvert qu’une famille de protéines essentielles au développement du cerveau, les IgSF-CAM, est beaucoup plus sévèrement touchée par les anomalies de la N-glycosylation. Cette avancée permet d’expliquer la susceptibilité du cerveau aux CDG, et de mieux comprendre le mécanisme d’autres maladies neurodéveloppementales telles que la déficience intellectuelle.
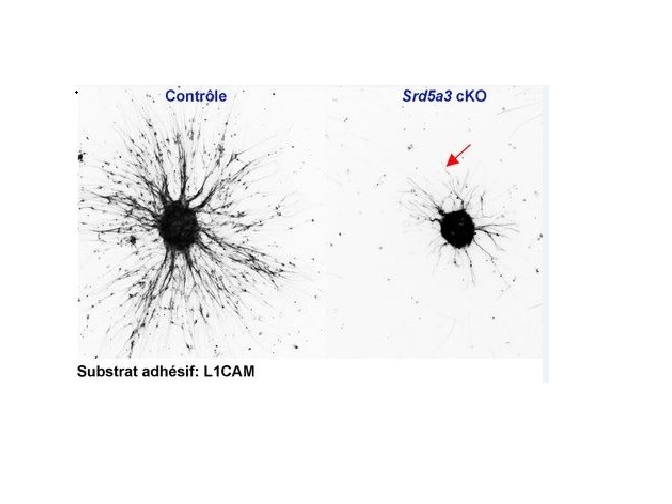
Culture de neurones en grain de cervelet de souris contrôles et mutantes (Srd5a3 cKO). Ces neurones émettent de longs et nombreux prolongements, les neurites, qui sont marqués avec un marquage ß-III tubuline. Les neurones de souris présentant un défaut de N-glycosylation ne produisent qu’un faible nombre de neurites courts (flèche rouge) en présence d’un support de culture de type L1CAM.
Les syndromes CDG ont une prévalence estimée à près de 1-2 enfants sur 100 000 naissances. Plusieurs gènes sont en cause dans ces pathologies et les symptômes peuvent être très variés. La majorité des patients présentent une maladie essentiellement neurologique avec la présence de trouble de l’équilibre, un retard psychomoteur et fréquemment une déficience intellectuelle.
Ces syndromes sont causés par un défaut lors de l’ajout de sucres sur nos protéines, ce qu’on appelle la N-glycosylation. Ces sucres jouent généralement un rôle clé en rendant la protéine stable ou en servant de signal lui permettant d’être fonctionnelle dans la cellule.
Afin de mieux comprendre pourquoi le développement cérébral est nettement plus sensible au défaut métabolique mis en cause dans les syndromes CDG, l’équipe de chercheurs a créé un modèle murin qui reproduit l’anomalie métabolique dans une partie du cerveau particulièrement touchée chez les patients, le cervelet. Elle a reproduit l’effet de mutations du gène Srd5a3, nécessaire à l’initiation du processus de glycosylation, tout en utilisant une approche de protéomique* pour observer la glycosylation des protéines dans leur ensemble. Cette approche a pu être réalisée grâce à une collaboration étroite avec la plateforme de protéomique de l’Hôpital Necker-Enfants malades/INEM-AP-HP.
L’équipe a constaté que toutes les protéines qui doivent être glycosylées ne sont pas affectées de la même façon. En effet, seules les protéines qui nécessitent de nombreux ajouts de sucre sont sévèrement touchées. Parmi elles, la famille des IgSF-CAM, qui est très abondante et essentielle pour le cerveau en développement. Ces protéines, localisées à la surface des cellules, ont un rôle prépondérant dans l’interaction des cellules avec leur environnement et les autres cellules qui les entourent. Des membres de cette famille ont un impact sur le développement des neurones et sont aussi impliqués dans d’autres maladies neurodéveloppementales telles que la déficience intellectuelle.
Selon le chercheur Daniel Medina-Cano, premier auteur de la publication, « ce travail montre qu’une anomalie touchant un processus indispensable à toutes les cellules ne les affecte pas de la même façon, et que toutes les protéines ne sont pas égales face à ces défauts. Ainsi le niveau de glycosylation joue un rôle clef dans la régulation de la famille de protéines IgSF-CAM ».
Ces progrès ont permis de mieux comprendre les mécanismes à l’origine des anomalies neurodéveloppementales des patients CDG et d’identifier chez la souris des marqueurs de la maladie, qui vont être utilisés pour tester certaines molécules, et ainsi améliorer le processus de glycosylation.
Au cours de ces travaux de recherche, une cartographie détaillée de la glycosylation lors du développement du cerveau a été générée, chose qui n’avait jamais été faite auparavant. Ces informations permettent de mieux comprendre le fonctionnement de nombreuses protéines, dont certaines sont associées à d’autres pathologies telles que l’autisme, la déficience intellectuelle ou l’épilepsie.
Ces travaux font l’objet d’une publication dans eLife, « High N-glycan multiplicity is critical for neuronal adhesion and sensitizes the developing cerebellum to N-glycosylation defect », publiée le 12 octobre 2018.
Plus d’informations ici sur l’équipe des Dr Vincent Cantagrel et Laurence Colleaux
*Protéomique : science qui étudie l’ensemble des protéines d’une cellule, d’un tissu, d’un organe ou d’un organisme à un moment donné, sous des conditions données.
Les quelques 9000 maladies génétiques recensées touchent 35 millions de patients en Europe, et près de 3 millions en France, où l’on compte chaque année 30 000 nouveaux cas. Près de 60 % des enfants reçus en consultation repartent sans diagnostic génétique et 90 % des maladies génétiques n’ont pas encore de traitement curatif. Face à cette problématique majeure de santé publique, le défi est double : diagnostiquer et guérir.
www.institutimagine.org

